Cục Quản lý Dược yêu cầu thay thế thuốc Bupivacaine sau tai biến sản khoa
- Đình chỉ thuốc dị ứng và thuốc mát gan giải độc
- Cục Quản lý Dược yêu cầu Cần Thơ "truy tìm" công văn thay thế thuốc gây tê
- Đình chỉ lưu hành thuốc PASAPIL do kém chất lượng
Theo Cục Quản lý Dược, trước đó Cục nhận được Văn bản số 219/SYT-NVD ngày 22-11-2019 của Sở Y tế Hà Nội về việc cung ứng mặt hàng Bupivacaine.
Tại văn bản trên, Sở Y tế Hà Nội có gửi kèm Văn bản số 1937/CPC1-KD ngày 21-11-2019 của Công ty cổ phần Dược phẩm Trung ương CPC1 thông báo gửi các cơ sở y tế về việc Công ty dừng xuất và đề nghị Bệnh viện tạm dừng sử dụng mặt hàng thuốc Bupivacaine WPW Spinal Heavy 0,5% (Số Giấy đăng ký lưu hành: VN-20879-17) do Công ty Warsaw Pharmaceutical Works Polfa S.A., Ba Lan sản xuất.
Liên quan đến nội dung này, Cục Quản lý Dược yêu cầu Công ty cổ phần Dược phẩm Trung ương CPC1 khẩn trương có giải pháp thay thế thuốc Bupivacaine WPW Spinal Heavy 0,5% đã trúng thầu để đảm bảo thực hiện hợp đồng đã ký kết theo quy định của Luật Đấu thầu 2013, Nghị định số 63/2014/NĐ-CP ngày 26-6-2014 và Thông tư số 15/2019/TT-BYT ngày 11-7-2019 của Bộ Y tế và đảm bảo nhu cầu khám bệnh, chữa bệnh của nhân dân.
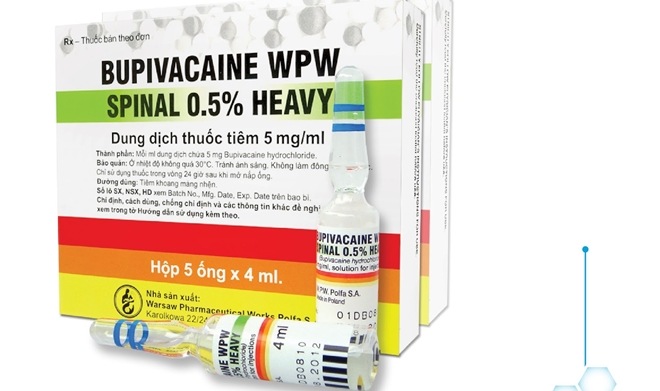 |
| Thuốc Bupivacaine WPW Spinal 0,5% Heavy |
Đồng thời, khẩn trương phối hợp với các đơn vị chức năng triển khai các nội dung theo chỉ đạo của Cục Quản lý Dược tại Công văn số 19671/QLD-ĐK và 19639/QLD-CL ngày 21-11-/2019. Yêu cầu Công ty gửi báo cáo bằng văn bản nội dung mục 1 về Cục Quản lý Dược.
Như Báo CAND đã đưa tin, liên tiếp trong thời gian qua, nhiều ca tai biến sản khoa sau khi gây tê mổ bắt con, đặc biệt là 3 ca ở Đà Nẵng nghi có liên quan đến thuốc gây tê Bupivacaine. Dư luận rất lo lắng, đặc biệt là tại các tỉnh miền Trung và phía Nam, nơi trúng thầu thuốc gây tê này. Sở Y tế Đà Nẵng và Sở Y tế Quảng Nam đã ngừng sử dụng thuốc Bupivacine.
Trước đó, Cục Quản lý Dược đã có công văn hỏa tốc gửi các Sở Y tế kèm danh sách 181 loại thuốc gây tê trúng thầu và 18 loại thuốc tiêm gây tê chứa Bupivacaine được đăng ký lưu hành còn lực.
Trong trường hợp cần thay thế thuốc đã trúng thầu, các đơn vị phải chủ động liên hệ với các cơ sở kinh doanh đã được Cục Quản lý Dược cung cấp trên để nhập khẩu thuốc kịp thời, đảm bảo đủ thuốc sử dụng.
