Bộ Y tế nói gì về đề xuất cấp phép khẩn cấp vaccine Nanocovax?
Theo ông Nguyễn Ngô Quang, Phó cục trưởng Cục Khoa học công nghệ và Đào tạo, Bộ Y tế, ông chỉ biết thông tin Nanogen xin cấp phép khẩn cấp có điều kiện vaccine Nanocovax qua báo chí.
Ông Quang khẳng định:“Nanogen gửi thẳng đề xuất lên Thủ tướng Chính phủ, không thông qua Bộ Y tế. Nếu theo đúng quy trình Nanogen phải gửi lên Bộ Y tế để chúng tôi xem xét, góp ý.
Ở thời điểm này, chưa có đầy đủ dữ liệu khoa học để đề xuất cấp phép khẩn cấp hay không cho vaccine Nanocovax. Việc cấp phép sử dụng vaccine luôn phải đảm bảo 3 yếu tố an toàn, sinh miễn dịch và hiệu lực bảo vệ. Vaccine là sản phẩm y tế đặc biệt”.
Ông Quang cũng cho biết thêm, hiện vaccine Nanocovax còn đang còn trong quá trình nghiên cứu, thử nghiệm, chưa kết thúc quá trình thử nghiệm nên chưa có dữ liệu đánh giá tổng quan.
Theo ông Quang, vaccine Nanocovax đã đi qua giai đoạn 2 của cuộc thử nghiệm và theo đánh giá có sinh miễn dịch rất tốt. Tuy nhiên, việc nghiên cứu mới chỉ ở cỡ mẫu vừa phải. Và hiện vaccine mới bước vào giai đoạn 3 và vừa tiêm xong mũi 1 cho 1.000 người trong số 13.000 người theo kế hoạch thử nghiệm.
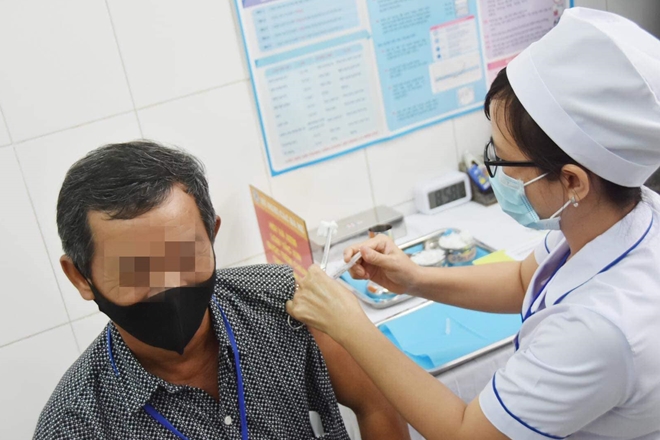 |
| Tiêm thử nghiệm lâm sàng vaccine Nanocovax giai đoạn 2 |
Theo kế hoạch, sau tiêm thử nghiệm mũi 2 (sau 28 ngày), cơ quan chuyên môn cần phải tiếp tục đánh giá sau các mốc 36, 45, 56 ngày sau tiêm. Trên cơ sở đó mới đủ tiêu chuẩn đánh giá tính sinh miễn dịch và hiệu lực bảo vệ của vaccine.
"Ít nhất phải sau 2 tháng và thử nghiệm trên cỡ mẫu đủ lớn mới có thể đánh giá để quyết định phê duyệt cấp phép khẩn cấp cho vaccine này hay không", ông Quang nói.
Trong khi Bộ Y tế cho rằng Nanogen khá vội vàng khi đề nghị cấp phép khẩn cấp với vaccine Nanocovax đang trong giai đoạn thử nghiệm 3, ông Hồ Nhân, Tổng Giám đốc Công ty Nanogen cho biết: "Đề xuất này không vội, vì vaccine phòng COVID-19 của các quốc gia khác như Nga, Ấn Độ, Trung Quốc cũng cấp phép khẩn cấp trong giai đoạn tương tự. Thậm chí sau giai đoạn 2 với tiêm thử nghiệm 200-300 người. Với vaccine Nanocovax hiệu quả được chứng minh ở pha 2. Máu của người tình nguyện đã trung hòa virus theo kết quả của Viện Pasteur TP Hồ Chí Minh...".
Trước đó, vào chiều qua 22/6, ông Hồ Nhân xác nhận việc đơn vị đã có công văn gửi Thủ tướng Chính phủ xin cấp phép khẩn cấp có điều kiện với vaccine phòng COVID-19 Nanocovax.
Nanocovax đang trong giai đoạn thử nghiệm lâm sàng thứ 3. Qua 2 giai đoạn đầu, kết quả thử nghiệm cho thấy, 100% tình nguyện viên đều sinh miễn dịch tốt. Tỷ lệ chuyển đổi huyết thanh đạt trên 99%. Bước đầu của giai đoạn 3 tiêm trên 1 nghìn mẫu cũng cho thấy kết quả khả quan.
Theo đại diện Nanogen, so với các loại vaccine khác trên thế giới là không hề thua kém và có phần cao hơn. Dù vậy, giá bán dự kiến của loại vaccine này cũng đang thấp nhất thế giới, chỉ với giá 120 nghìn đồng/liều vaccine.
Công suất sản xuất hiện nay của Nanogen đạt 8 triệu – 12 triệu liều/tháng, đơn vị cũng đang hoàn thiện và mở rộng hệ thống kho lạnh, đảm bảo lưu trữ 10 triệu liều.
Dự kiến, Nanogen có thể cung cấp 50 triệu liều đến tháng 12/2021 và 100 triệu liều vào năm 2022..., đảm bảo cung cấp đủ vaccine để Việt Nam đạt được miễn dịch cộng đồng vào quý II/2022.
