Tước giấy chứng nhận 2 Công ty Dược vi phạm
- Rút giấy phép 2 công ty dược nước ngoài
- TP HCM: Công ty Dược bán thuốc "quá đát"
- Tổng Giám đốc Công ty Dược phẩm Viễn Đông chờ ra tòa
Theo đó, đơn vị bị xử phạt nhiều nhất là Công ty Cổ phần sinh học Dược phẩm Ba Đình (Quế Võ-Bắc Ninh) với số tiền 150 triệu đồng do sản xuất thuốc viên nén Misoprostol (là thuốc gây sảy thai), SĐK: VD-20509-14, số lô 0207, HD: 20/03/2020 không đạt chất lượng.
Không chỉ thế, Công ty này còn vi phạm khi không báo cáo với cơ quan có thẩm quyền khi có thay đổi; không thực hiện đúng quy trình thao tác chuẩn trong quá trình sản xuất thuốc đã đăng ký và không thực hiện đúng quy định về điều kiện bảo quản nguyên liệu misoprotol trong quá trình bảo quản.
Vì thế, cùng với xử phạt tiền, Cục Quản lý Dược còn yêu cầu Công ty Cổ phần sinh học Dược phẩm Ba Đình thu hồi và tiêu hủy toàn bộ lô thuốc không đạt chất lượng trên, để báo cáo về Cục Quản lý Dược sau 10 ngày hoàn tất thủ tục hủy thuốc.
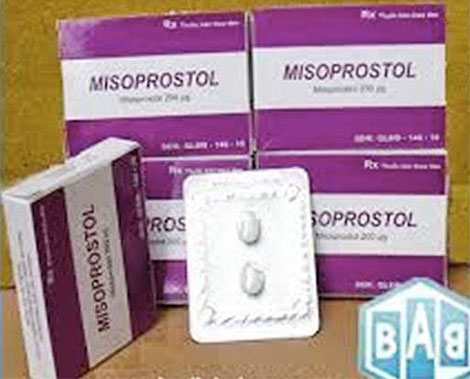 |
| Thuốc viên nén Misoprostol không đạt chất lượng. |
Công ty này cũng phải thu hồi nguyên liệu Misoprostol bảo quản không đúng điều kiện của nhà sản xuất ghi trên nhãn, đồng thời, gửi nguyên liệu Misoprostol bảo quản không đúng điều kiện đến các cơ sở đạt GLP của nhà nước để kiểm nghiệm và báo cáo kết quả kiểm nghiệm về Cục Quản lý Dược. Chỉ sau khi nguyên liệu misoprostol khi đạt tiêu chuẩn chất lượng như trong hồ sơ đăng ký thuốc đã được Cục Quản lý Dược phê duyệt Công ty mới được phép sử dụng lại nguyên liệu này.
Ngoài ra, Cục Quản lý Dược còn tước quyền sử dụng Giấy chứng nhận đủ điều kiện kinh doanh thuốc do Bộ Y tế cấp cho Công ty Cổ phần sinh học Dược phẩm Ba Đình trong thời gian 3 tháng.
85 triệu đồng là số tiền mà Cục Quản lý Dược xử phạt Công ty TNHH L- Beauty Việt Nam (quận 1, TP Hồ Chí Minh) do kinh doanh mỹ phẩm “sản phẩm Dior Homme Sport very cool spray fresh eau de toillete và Dior J’Adore L’or Essence de Parfum” có công thức không đúng với hồ sơ công bố đã được phê duyệt, đồng thời, quảng cáo mỹ phẩm chưa được cơ quan có thẩm quyền xác nhận nội dung.
Cục Quản lý Dược còn yêu cầu Công ty TNHH L- Beauty Việt Nam thu hồi và tiêu hủy sản phẩm mỹ phẩm trên và tháo gỡ nội dung quảng cáo vi phạm.
Công ty TNHH dược phẩm USAPHA (Tiên Du- Bắc Ninh) bị Cục Quản lý Dược xử phạt 40 triệu đồng do sản xuất sản phẩm không phải là thuốc trên dây chuyền sản xuất thuốc.
Cục Quản lý Dược cũng yêu cầu Công ty TNHH dược phẩm USAPHA thu hồi thuốc Livganic, SĐK: QLĐB -517-17, số lô 0117, NXS: 4-4-2017, HD: 4-4-2020, gửi các mẫu thuốc đến các cơ sở đạt GLP của nhà nước để kiểm nghiệm, báo cáo kết quả kiểm nghiệm về Cục Quản lý Dược. Công ty này chỉ được phép lưu thông thuốc Livganic khi đạt tiêu chuẩn chất lượng như trong hồ sơ đăng ký thuốc đã được phê duyệt.
Bên cạnh xử phạt 40 triệu đồng, Cục Quản lý Dược còn tước quyền sử dụng Giấy chứng nhận đủ điều kiện kinh doanh thuốc do Bộ Y tế cấp trong thời gian 4,5 tháng đối với công ty TNHH dược phẩm USAPHA.
